Клетки Купфера, или резидентные макрофаги печени
Авторы: Лаура Дж. Диксон, Марк Барнс, Хуэй Тан, Мишель Т. Притчард и Лаура Э. Наджи
Пер. с англ. Н.Д. Фирсовой, 2018
Физиология клеток Купфера
Клетки Купфера, резидентные макрофаги печени, представляют собой наибольшую совокупность резидентных тканевых макрофагов в организме. Впервые описаны Карлом Вильгельмом фон Купфером в 1876 году как «стернцелен» (звездные или звездчатые клетки), эти клетки вначале считались частью эндотелия сосудов печени. Только в 1898 году Тадеуш Бровец правильно определил их как макрофаги.
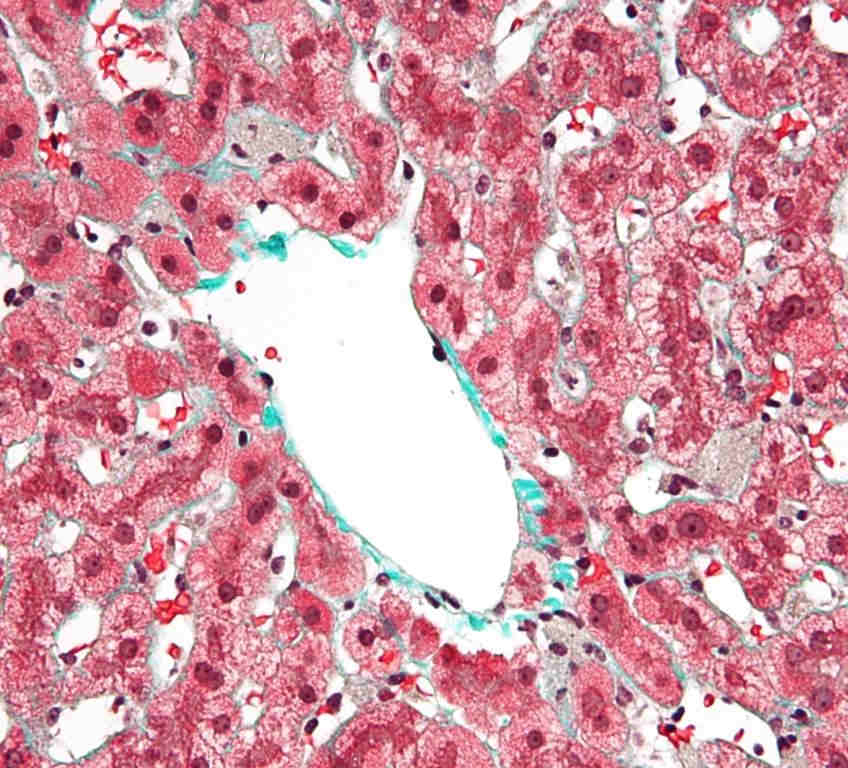
Клетки Купфера играют решающую роль во врожденном иммунном ответе; локализация в печеночном синусоиде позволяет им эффективно фагоцитировать патогены, поступающие с портальным или артериальным кровотоком. Клетки Купфера также служат первой линией защиты от иммунореактивного материала, попадающего с портальной циркуляцией из желудочно-кишечного тракта, и могут считаться конечным компонентом барьерной функции кишечника. Таким образом, клетки Купфера играют основную противовоспалительную роль, предотвращая продвижение иммунореактивных веществ, поступающих из кишечника, через печеночные синусоиды. Клетки Купфера также отлично справляются с функцией устранения частиц, таких как погибшие эритроциты и другие клетки, попадающих в паренхиму печени из системного кровообращения. Таким образом, клетки Купфера представляют собой основную фагоцитарную активность того, что классически называли ретикулярно-эндотелиальной системой, а теперь более правильно называют мононуклеарной фагоцитарной системой.
Изменение функциональной активности клеток Купфера связано с различными болезненными состояниями. В то время как клетки Купфера могут быть защитой в ряде ситуаций, включая лекарственное повреждение печени и индуцированный токсинами фиброз; дисрегуляция воспалительных реакций в клетках Купфера может способствовать хроническому воспалению в печени, включая алкогольную и безалкогольную жировую болезнь печени – НЖБП/НАСГ (НЖБП – неалкогольная жировая болезнь печени, НАСГ – неалкогольный стеатогепатит).
Происхождение клеток Купфера
У взрослых животных незрелыми предшественниками тканевых макрофагов считаются моноциты в периферическом кровообращении, происходящие из клеток-предшественников в костном мозге. Моноциты периферической крови могут проникать в печень, а затем созревать в фенотип, характерный для тканевых макрофагов. Дифференциация макрофагов регулируется различными факторами роста, но наиболее важной для развития зрелых клеток Купфера представляется роль макрофагального колониестимулирующего фактора.
Контроль количества клеток Купфера в печени тесно поддерживается; однако механизмы этого контроля недостаточно понятны. Ясно, что скорость поступления периферических моноцитов в печень выше, чем в другие ткани, например, в легкие; однако существует противоречие, касающееся периода жизни клеток Купфера в печени. Исследования, проведенные на животных, в ходе которых клетки Купфера истощали либо клодронатом, либо трансплантацией костного мозга, показывают, что их замена происходит через 14-21 день. Однако судьба клеток Купфера в физиологических условиях еще не понята; предполагается, что их оборот может произойти из-за запрограммированной гибели (апоптоза) и/или миграции на другие участки, например, в лимфатические узлы. Недавно полученные данные показывают, что в ответ на Th-2 воспалительные сигналы, такие как увеличение IL-4, может стимулироваться пролиферация резидентных макрофагов, в том числе клеток Купфера.
Локализация клеток Купфера в печеночной архитектуре
Печень представляет собой сложный орган, состоящий из ряда высокоспециализированных типов клеток, которые распределены внутри синусоидальной структуры печени. Гепатоциты, которые составляют основную массу печени, считаются рабочими лошадками и выполняют широкий спектр метаболических, регуляторных и токсикологических функций. Печеночная синусоида выстилается специализированными печеночными синусоидальными эндотелиальными клетками, характеризующимися наличием фенестр (окон). Внутри синусоиды находятся клетки Купфера, а также другие клетки врожденной иммунной системы, включая естественные киллеры, естественные киллеры-Т-клетки и дендритные клетки. Близость клеток Купфера к паренхиматозным и непаренхиматозным клеткам печени поддерживает способность клеток Купфера регулировать функцию печени, как в здоровом состоянии, так и в болезни. В здоровой печени клетка Купфера демонстрирует то, что было названо «толерогенным» фенотипом. Эта толерантность необходима для предотвращения нежелательных иммунных реакций в отношении входящих в печеночную синусоиду иммунореактивных веществ, включая материалы, полученные из кишечника, а также антигены, присутствующие в мертвых или умирающих клетках, поскольку в печени они удаляются из кровообращения.
Однако при определенных болезненных состояниях клетка Купфера переходит из этого толерогенного фенотипа в патологически активированное состояние, которое характерно для хронических воспалительных заболеваний. Учитывая тесную близость клетки Купфера к паренхиматозным и непаренхиматозным клеткам печени, потеря толерантного состояния может привести к повреждению гепатоцеллюлярной ткани. Таким образом, как и в случае многих других компонентов врожденной иммунной системы, поддержание соответствующей функциональной активности клеток Купфера имеет решающее значение для поддержания организма в здоровом состоянии.
Отсутствие или пониженная функциональная активность клеток Купфера может способствовать инвазии патогенов и/или системному воспалению. Напротив, активация клеток Купфера в таких условиях, как НЖБП/НАСГ, приводит к неконтролируемому воспалению печени. Поэтому при создании терапевтических средств, предназначенных для лечения хронических воспалительных заболеваний печени, крайне важно разработать подходы, которые нормализуют или подавляют, но не устраняют полностью функциональную активность клеток Купфера.
Пластичность печеночных макрофагов
Растет понимание того, что зрелый фенотип тканевых макрофагов-резидентов является очень пластичным, а функциональная активность макрофага, развивающаяся на основе ресурсов как местной метаболической, так и иммунной среды, накладывается на программу его внутренней дифференциации. В печени пластичность может быть результатом изменения состояния активации резидентных клеток Купфера и/или набора новых моноцитов/макрофагов в печень. Значительная часть нашего понимания пластичности макрофагов происходит от резидентных макрофагов жировой ткани и нетканевых макрофагов. Однако недавние данные подтверждают, что регуляция функционального фенотипа печеночных макрофагов связана с прогрессированием различных заболеваний печени, включая АБП (алкогольную болезнь печени), НАСГ, фиброз и гепатоцеллюлярную карциному.
Сейчас получен ряд доказательств, которые демонстрируют значительную гетерогенность активационных состояний макрофагов. В попытке классифицировать эти состояния активации, две крайние поляризации макрофагов обозначены как M1 и M2. M1, или классически активированные макрофаги характеризуются повышенной экспрессией провоспалительных цитокинов, включая TNF-α, IL-6, IL-12 и индуцируемую NO-синтазу (iNOS), тогда как M2, или альтернативно активированные макрофаги проявляют низкую экспрессию провоспалительных цитокинов, но повышенную экспрессию противовоспалительных медиаторов, таких как экспрессия рецептора IL-10 и IL1.
Классификация M1/M2 явно упрощена, данные показывают, что в каждой из этих групп существует значительная гетерогенность. Действительно, группа M2 была далее подразделена на M2a, M2b и M2c. Эти подклассы индуцируются различными регуляторами и проявляют различные маркерные белки на своей клеточной поверхности, так же, как и различную функциональную активность. Особый интерес для исследователей представили дополнительные фенотипы резидентных макрофагов в печени. Например, макрофаги, связанные со спонтанным разрешением фиброза печени, и названные шрам-ассоциированными макрофагами (SAM) группы Iredale.
Эти SAM представляют собой Gr-1hi и связаны с повышенной экспрессией профибротических цитокинов, трансформирующим фактором роста β (TGF-β) и тромбоцитарным фактором роста. Другой специфический фенотип макрофагов связан с гепатокарциномой. Эти связанные с опухолью макрофаги, преимущественно экспрессирующие фенотип М2, имеют отдельный транскрипционный профиль, который может способствовать усиленному ангиогенезу опухоли из-за повышенной экспрессии VEGF, который стимулирует ангиогенез, и матричных металлопротеаз, которые облегчают ангиогенную реконструкцию.
Наше понимание точных механизмов регуляции поляризации макрофагов по-прежнему очень рудиментарно, хотя в недавних исследованиях стали выясняться специфические факторы транскрипции, которые регулируют переключение, включая преобразователи сигналов и активаторы транскрипции (STAT), рецепторы, активируемые пероксисомными пролифераторами (PPAR), индуцируемый гипоксией фактор 2α и Круппель-подобный фактор 4. Сильные поляризационные факторы M1 включают STAT1 и интерферон-регуляторный фактор 5 (IRF), тогда как STAT6, IRF-4 и PPARγ являются важными факторами транскрипции, регулирующими поляризацию M2. МикроРНК также способствуют регуляции поляризации макрофагов в клеточных линиях культивируемых макрофагов; однако данные о роли микроРНК in vivo в регулировании фенотипа клеток Купфера по-прежнему отсутствуют. Сообщалось также о пролиферации макрофагов М2 в ответ на IL-4.
Также растет понимание того, что метаболическое состояние макрофага, в частности, использует ли он в качестве первичного источника топлива глюкозу или жирные кислоты, влияет на фенотипическую активность макрофага. Действительно, регуляторы метаболизма липидов, такие как члены семейства PPAR и адипонектин, являются важными регуляторами поляризации макрофагов. Многочисленные члены семейства PPAR вносят различный вклад в поляризацию M2, при этом PPARγ увеличивает окислительное фосфорилирование, а PPARδ регулирует экспрессию рецепторов распознавания образов и костимуляторных молекул. Точно так же полноразмерный адипонектин координирует экспрессию как PPARγ, так и PPARδ, генов, регулирующих окислительное фосфорилирование, и поляризацию M2. Эта двойная регуляция метаболизма липидов и поляризация макрофагов особенно интересна в свете вклада клеток Купфера и других печеночных макрофагов в прогрессирование метаболических заболеваний печени, таких как АБП и НАСГ, которые изначально характеризуются дисрегуляцией метаболизма липидов в печени.
Клетки Купфера при заболеваниях печени
Активация клеток Купфера необходима для ответа печени на инфекцию или травму; последующий воспалительный ответ защищает от инфекции, а также ограничивает клеточное и органное повреждение организма хозяина. Таким образом, во многих случаях, таких как интоксикация ацетаминофеном, а также при гепатоцеллюлярном восстановлении, клетка Купфера выполняет важную защитную, заживляющую функцию. Однако при других типах повреждений печени клетка Купфера неспособна надлежащим образом контролировать или разрешать свое состояние активации. Контролируемое и адекватное разрешение воспаления является важной особенностью врожденного иммунного ответа. Неспособность клеток Купфера разрешать активацию способствует возникновению ряда хронических воспалительных заболеваний печени. Учитывая двойную защитную и потенциально опасную роль активации клеток Купфера, разработка терапевтических стратегий для модуляции активности клеток Купфера во время болезни печени должна быть критически рассчитана таким образом, чтобы адекватно регулировать функцию клеток Купфера во время динамических стадий повреждения печени.
При исследовании роли клеток Купфера в здоровом состоянии и в болезни важно понять, что локализованный ответ врожденной иммунной системы в печени может отличаться от системного врожденного иммунного ответа и/или локализованных реакций других органов. Например, хроническое употребление алкоголя обычно повышает восприимчивость индивидуумов к инфекциям. Предположительно, несмотря на повышенные воспалительные реакции, наблюдаемые в печени в результате хронического употребления этанола, системные иммунные реакции подавляются хроническим воздействием этанола.
Даже внутри печени могут быть различными ответы отдельных компонентов иммунного ответа. Одним из примеров является взаимодействие этанола с инфекцией – вирусом гепатита С (HCV). Хроническое злоупотребление алкоголем связано с увеличением заболеваемости HCV -инфекцией. Уменьшенная способность отражать вирусные инфекции контрастирует с повышенным ответом печени на эндотоксин. Такие разные ответы могут быть связаны с высокоспецифическим толерантным статусом клетки Купфера в печени.
Понимание локализованных и специфических реакций иммунной системы в печени поможет разработать стратегии вмешательств, специально направленные на звенья иммунной системы, которые способствуют инициированию и поддержанию заболеваний печени.
Клетки Купфера способствуют метаболическим заболеваниям печени: алкогольная и неалкогольная болезнь печени
Прогрессирование АБП и НЖБП/НАСГ следует характеристикам, общим для всех типов заболеваний печени, независимо от этиологии. Эта прогрессия отмечена появлением жирового гепатоза, некроза гепатоцитов и апоптоза, воспаления, регенерирующих узелков, фиброза и цирроза. Развитие стеатоза, воспаления, фиброза и цирроза представляет собой сложный процесс, включающий как паренхиматозные, так и непаренхиматозные клетки печени, а также другие типы печеночных клеток в ответ на повреждение и воспаление. Многие из событий, связанных с развитием АБП или НЖБП/НАСГ, типичны для других ответных реакций тканей на повреждение, таких как заживление повреждений кожи и мягких тканей. Как и во всех ответах на заживление ран, врожденная иммунная система вносит решающий вклад в своевременное и эффективное восстановление как структуры, так и функции поврежденной ткани или органа. Действительно, в то время как развитие фиброза печени инициируется в ответ на гепатоцеллюлярное повреждение, дисрегуляторные воспалительные процессы способствуют развитию фиброзной болезни.
Особенно важную роль в развитии заболевания печени играют печеночные макрофаги. Роль клеток Купфера, резидентных печеночных макрофагов, была впервые определена как ключевой вклад в прогрессию АБП. В то время как ранние исследования ожирения характеризовали критическую роль резидентных макрофагов жировой ткани в развитии метаболического синдрома, более поздние исследования также идентифицировали клетки Купфера как важнейшие медиаторы НЖБП/НАСГ. Например, в модели с высоким содержанием жиров при печеночном стеатозе у мышей истощение клеток Купфера при помощи клодроната приводит к аннулированию стеатоза печени.
Распространенность АБП и НЖБП/НАСГ
Злоупотребление алкоголем является основной причиной заболеваемости и смертности во всем мире. Статистика показывает, что в США 18 миллионов американцев злоупотребляют алкоголем и что АБП затрагивает более 10 миллионов человек. В то время как жировой гепатоз встречается у 90% алкоголиков, лишь у немногих людей, регулярно употребляющих алкоголь, когда-либо развивались гепатит, фиброз и цирроз. Это указывает на роль генетических и экологических факторов риска, таких как факторы, влияющие на тяжесть стеатоза и окислительного стресса, цитокиновой среды, величины иммунного ответа и/или эпигенетической регуляции.
НЖБП – это спектр расстройств, которые включают стеатоз, стеатоз с воспалением, неалкогольный стеатогепатит (НАСГ) и НАСГ с фиброзом. Развитие НЖБП/НАСГ сильно связано с ожирением и метаболическим синдромом; в совокупности метаболический синдром характеризуется повышенным риском хронических заболеваний, включая инсулинорезистентность и диабет 2 типа, дислипидемию и сердечно-сосудистые заболевания, а также НЖБП/НАСГ.
Подобно темпам прогрессирования АБП, не у всех людей с ожирением развивается метаболический синдром и НЖБП/НАСГ, что указывает на роль экологических и/или генетических вкладов в прогрессирование повреждения печени. Например, от 10% до 29% пациентов с НАСГ достигнут цирроза в течение 10 лет, и ожидается, что у этих 4% до 27% будет развиваться гепатоцеллюлярная карцинома. Таким образом, продвинутая НЖБП, особенно НАСГ с фиброзом, представляет собой значительный риск развития цирроза и гепатоцеллюлярного рака.
Из-за своей высокой распространенности НЖБП может превзойти хронический гепатит C в качестве ведущего показания к трансплантации печени к 2020 году. Показатели ожирения достигают масштабов эпидемии во всем мире, и существует настоятельная необходимость понять патофизиологические механизмы повреждения тканей, вызванного ожирением, для выявления новых терапевтических целей и факторов риска прогрессирования ожирения в болезнь.
Хотя некоторые компоненты врожденного иммунного ответа участвуют в инициации и прогрессировании АБП и НЖБП / НАСГ, клетки Купфера, резидентные макрофаги печени, особенно важны для начала и развития хронического повреждения печени. Абляция клеток Купфера предотвращает развитие жирового гепатоза и воспаления у крыс, хронически подвергающихся воздействию этанола путем внутрижелудочного питания. Аналогичным образом, истощение клеток Купфера защищает от развития печеночной инсулинорезистентности и стеатоза печени, вызванных диетой с высоким содержанием жиров.